(Trang 85)
I. HỆ THỐNG HOÁ KIẾN THỨC
CẶP OXI HOÁ - KHỬ CỦA KIM LOẠI
Dạng oxi hoá (Mn+) và dạng khử (M) của cùng một kim loại tạo nên cặp oxi hoá - khử, giữa chúng có mối quan hệ: Mn+ + ne M
THẾ ĐIỆN CỰC CHUẨN
Khái niệm
Thế điện cực chuẩn là đại lượng đánh giá khả năng khử giữa các dạng khử và khả năng oxi hoá giữa các dạng oxi hoá ở điều kiện chuẩn.
Ý nghĩa
- Giá trị thế điện cực chuẩn của cặp oxi hoá - khử Mn+/M càng lớn thì tính oxi hoá của ion Mn+ càng mạnh và tính khử của kim loại M càng yếu và ngược lại.
- Phản ứng hoá học giữa hai cặp oxi hoá - khử xảy ra theo chiều: Chất oxi hoá của cặp oxi hoá - khử có thế điện cực chuẩn lớn hơn oxi hoá chất khử của cặp oxi hoá - khử có thế điện cực chuẩn nhỏ hơn.
NGUỒN ĐIỆN HOÁ HỌC
Pin Galvani
- Pin Galvani có cấu tạo gồm hai điện cực, mỗi điện cực ứng với một cặp oxi hoá - khử và thường nối với nhau qua cầu muối.
- Ở anode xảy ra quá trình oxi hoá, còn ở cathode xảy ra quá trình khử.
- Sức điện động chuẩn của pin: Eopin = Eocathode - Eoanode
Một số nguồn điện khác
- Acquy thuộc loại pin sạc, được sử dụng phổ biến trong nhiều loại ô tô.
- Pin nhiên liệu và pin Mặt Trời là những nguồn năng lượng sạch, tiềm năng.
ĐIỆN PHÂN
Thứ tự điện phân
- Tại anode, chất khử mạnh hơn bị oxi hoá trước.
- Tại cathode, chất oxi hoá mạnh hơn bị khử trước.
Ứng dụng
- Nhôm được sản xuất bằng phương pháp điện phân nóng chảy:
2Al2O3 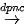 4Al + 3O2
4Al + 3O2
- Đồng được tinh luyện bằng phương pháp điện phân với anode bằng đồng thô.
- Mạ điện được sử dụng để trang trí bề mặt hoặc bảo vệ kim loại khỏi sự ăn mòn.
(Trang 86)
I. LUYỆN TẬP
Câu 1. Xét các cặp oxi hoá - khử sau:
| Cặp oxi hoá - khử | Al3+/AI | Ag+/Ag | Mg2+/Mg | Fe2+/Fe |
| Thế điện cực chuẩn (V) | -1,676 | +0,799 | -2,356 | -0,44 |
a) Kim loại có tính khử mạnh nhất, yếu nhất lần lượt là
A. Mg, Ag.
B. Al, Ag.
C. Al, Fe.
D. Mg, Fe.
b) Số kim loại khử được ion H+ thành khí H2 ở điều kiện chuẩn là
A. 1.
B. 2.
C. 3.
D. 4.
c) Số kim loại khử được ion Ag+ thành Ag ở điều kiện chuẩn là
A. 4.
B. 1.
C. 3.
D.2.
Câu 2. Cho pin điện hoá tạo bởi hai cặp oxi hoá - khử ở điều kiện chuẩn: Pb2+/Pb và Zn2+/Zn với thế điện cực chuẩn tương ứng là –0,126 V và –0,762 V.
a) Xác định anode, cathode của pin điện.
b) Viết quá trình xảy ra ở mỗi điện cực và phương trình hoá học của phản ứng xảy ra khi pin hoạt động.
c) Xác định sức điện động chuẩn của pin.
Câu 3. Sức điện động chuẩn của pin điện hoá gồm hai điện cực M2+/M và Ag+/Ag bằng 1,056 V.
Trong số các kim loại Cu, Fe, Ni, Sn:
a) Hãy cho biết kim loại nào phù hợp với M.
b) Lựa chọn kim loại M để pin điện hoá có sức điện động chuẩn lớn nhất.
Cho biết:
| Cặp oxi hoá - khử | Fe2+/Fe | Ni2+/Ni | Sn2+/Sn | Cu2+/Cu | Ag+/Ag |
| Thế điện cực chuẩn (V) | -0,44 | -0,257 | -0,137 | +0,340 | +0,799 |